Trennverfahren
Trennverfahren sind physikalische Vorgänge, beim Trennen wird die chemische Zusammensetzung der Stoffe nicht verändert. Die einzelnen Reinstoffe eines Gemenges können somit abgetrennt werden, ohne dass diese Reinstoffe verändert werden. Einige dieser Trennverfahren werden in diesem Kapitel vorgestellt.
1. Sedimentieren
2. Dekantieren
3. Filtrieren
4. Zentrifugieren
5. Abscheiden
6. Abdampfen
7. Extrahieren
8. Destillieren
9. Chromatografieren
10. Trennung mittels eines Magneten
1. Sedimentieren
Unter Sedimentieren
versteht man das Absinken von feinen unlöslichen Feststoffteilchen in einer
Flüssigkeit.
Beispiel:
Wenn man etwa einen Teelöffel Gartenerde in einem Glas Wasser umrührt, kann man beobachten, dass in dem bräunlichen Gemisch größere Teilchen schnell zu Boden sinken. Wenn man das Gemisch einen Tag stehen lässt, so haben sich auch die leichtesten Teilchen am Glasboden abgesetzt (sedimentiert). Die darüber stehende Flüssigkeit ist klar.
2. Dekantieren
Unter Dekantieren
versteht man das Abgiessen einer Flüssigkeit, welche sich über einem
unlöslichen Feststoff oder einer unlöslichen Flüssigkeit befindet.
Beispiele:
- Das Fett einer Soße kann man mit etwas Geschick größtenteils abgießen (dekantieren).
- Kaffee kann vom Kaffeesatz abgegossen (dekantiert) werden.

- Wasser kann man
größtenteils von Sand abtrennen.
Aus diesen Beispielen kann man schon erkennen, dass die Dekantation keine
sehr genaue Trennmethode ist.
3. Filtrieren
a. Normale Filtration.
Durch eine Filtration kann man eine Flüssigkeit von einem in ihr unlöslichen
Feststoff trennen.

Um ein Gemisch zu
filtrieren, gießt man das Gemisch durch ein Sieb oder ein Filterpapier.
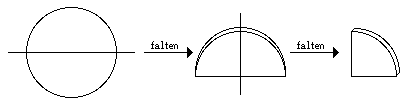
Falten des Filterpapiers:
Die Flüssigkeit, welche
aus sehr kleinen Teilchen besteht, fließt problemlos durch die Poren des
Filterpapiers. Man bezeichnet die austretende Flüssigkeit als Filtrat. Der
unlösliche Feststoff besteht aus Teilchen, die größer sind als die Poren des
Filterpapiers. Der Feststoff bleibt im Filterpapier zurück, man bezeichnet
diesen Feststoff als Niederschlag.
Beispiel:
Filtration eines Wasser-Sand-Gemisches.
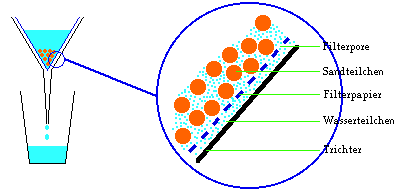
Die Filtration beruht also auf der unterschiedlichen Größe der zu filtrierenden Stoffteilchen.
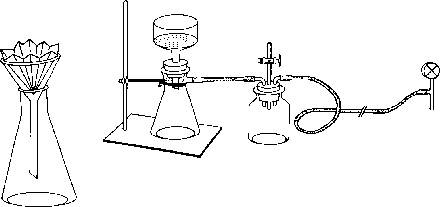
b. Filtration unter
vermindertem Druck.
Obwohl die normale Filtration die Trennung eines heterogenen Gemisches aus
einer Flüssigkeit und einem darin unlöslichen Feststoff erlaubt, besitzt sie
zwei große Nachteile:
- die Filtration verläuft relativ langsam
- eine vollständige Trennung ist fast unmöglich, es bleibt immer noch etwas
Flüssigkeit am Niederschlag haften.
Unter vermindertem Druck verläuft eine solche Filtration wesentlich
schneller, auch wird durch den Unterdruck Luft durch den Niederschlag
gesogen und dadurch getrocknet.
Beispiel:
Filtration eines Wasser-Sand-Gemisches.
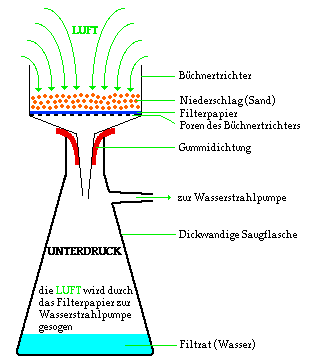
Der verminderte Druck
wird durch eine Wasserstrahlpumpe erreicht. In der Wasserstrahlpumpe reißt
ein feiner Wasserstrahl Luftteilchen mit sich. Schließt man die
Wasserstrahlpumpe an die Saugflasche an, so werden Luftteilchen aus der
Saugflasche angesogen. Dadurch entsteht in der Saugflasche ein Unterdruck:
- Befindet sich noch Flüssigkeit im Büchnertrichter so wird sie sehr schnell
in die Saugflasche eingesogen, um den Druck auszugleichen: Die Filtration
unter vermindertem Druck verläuft wesentlich schneller als eine normale
Filtration.
- Befindet sich nur noch ein wenig Restflüssigkeit im Büchnertrichter, so
wird Luft aus der Umgebung durch den Niederschlag und das Filterpapier in
die Saugflasche eingesogen. Dadurch wird der Niederschlag getrocknet.
4. Zentrifugieren
Wenn man einen sehr
fein verteilten, unlöslichen Feststoff aus einer Flüssigkeit filtrieren
will, so ist die normale Filtration unbrauchbar, da die Filtration äußerst
langsam verläuft, und die Poren des Filterpapiers oft verstopfen.
Aber auch eine Filtration unter vermindertem Druck hilft hier nicht weiter,
da wiederum die Poren des Filters verstopfen, und unter Umständen das
Filterpapier reißt, und eine Filtration daher nicht möglich ist.
In einem solchen Fall kann eine Zentrifugation weiterhelfen. Dazu braucht
man einen speziellen Apparat, eine Zentrifuge. Eine Zentrifuge besteht
hauptsächlich aus einer Achse, an der man - an zwei beweglichen Seitenarmen
- dickwandige Reagenzgläser anbringen kann.
Beispiel:
Zentrifugation eines Wasser-Gartenerde-Gemisches.
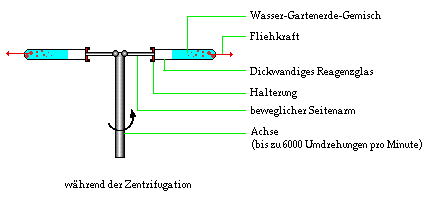
Schließt man den Apparat an, so dreht sich die Achse sehr schnell, bis zu 6000 Umdrehungen pro Minute. Durch die Fliehkraft werden die Reagenzgläser an den beweglichen Seitenarmen in die Waagerechte gebracht. Auch durch die Fliehkraft bedingt, verläuft die Flüssigkeit nicht. Die Fliehkraft drückt die Feststoffteilchen fest an den Boden des Reagenzglases. Da dies bei hohem Druck geschieht, bleiben die Feststoffteilchen auch noch nach der Zentrifugation am Boden haften.

Nach dem Lösen der Reagenzgläser aus der Halterung, kann man die Flüssigkeit dekantieren, ohne Feststoffteilchen mitzureißen, da die Feststoffteilchen sehr fest am Boden des Reagenzglases haften.
5. Abscheiden
Durch Abscheiden in
einem Scheidetrichter kann man zwei ineinander unlösliche Flüssigkeiten
trennen.
Vermengt man beide Flüssigkeiten eng miteinander, dann bildet sich ein
heterogenes Gemisch, welches man als
Emulsion bezeichnet. Gibt man
das Gemisch in einen Scheidetrichter, dann trennen sich die beiden
Flüssigkeiten, und man erhält zwei Phasen: Die untere Phase enthält immer
die Flüssigkeit mit der größten
Dichte, die obere Phase wird
immer durch die Flüssigkeit mit der kleineren Dichte gebildet. Durch Öffnen
des Hahnes kann man die untere Phase von der oberen Phase trennen.
Beispiel:
Ein Öl-Wasser-Gemenge.
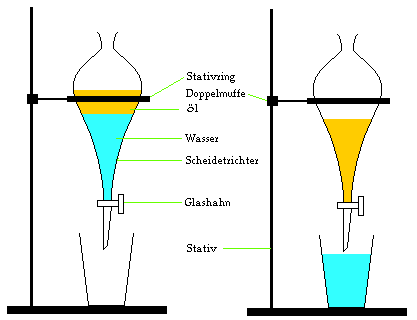
Öl besitzt eine kleinere Dichte als Wasser und bildet daher die obere Phase im Scheidetrichter. Wasser bildet die untere Phase.
6. Abdampfen
Durch Abdampfen eines
homogenen Gemisches (löslicher Feststoff in einer Flüssigkeit) kann man den
löslichen Feststoff von der Flüssigkeit trennen. Die Flüssigkeit geht aber
bei diesem Vorgehen durch Verdampfen verloren.
Beispiel:
Ein homogenes Salz-Wasser-Gemenge.
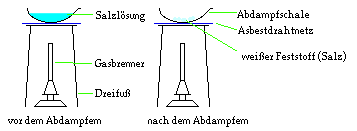
Nach dem Verdampfen des Wassers bleibt Salz als weißer Feststoff zurück.
7. Extrahieren
Unter Extrahieren
versteht man das Herauslösen von Stoffen mithilfe eines
Lösungsmittels.
Man kann sowohl
- eine bestimmte Flüssigkeit aus einer anderen Flüssigkeit herauslösen, als
auch
- lösliche Feststoffe aus Flüssigkeiten oder aus anderen Feststoffen
herauslösen.
Dieses Verfahren beruht auf der unterschiedlichen Löslichkeit der einzelnen
Stoffe. Eine Extraktion kann man in einem Scheidetrichter durchführen.
Beispiele:
Aufbereiten von Kaffee oder Tee. Dabei werden wasserlösliche Stoffe aus dem
Kaffeepulver beziehungsweise aus dem Tee herausgelöst.
Eine Wasser-Ether Extraktion, um einen in Wasser schwer löslichen Stoff in
die Etherphase zu überführen, in welchem der Stoff sehr löslich ist.
8. Destillieren
a) einfache
Destillation
Mit einer einfachen Destillation kann man sehr leicht lösliche Feststoffe
von einem Lösungsmittel trennen. Für Flüssigkeiten mit sehr großen
Siedetemperaturunterschieden ist auch eine Trennung möglich.
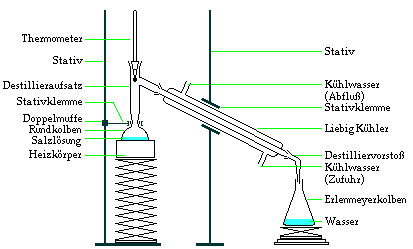
In einem ersten Schritt wird das Stoffgemenge langsam erhitzt. Die
Flüssigkeit mit der kleinsten Siedetemperatur steigt als Erste als Dampf in
dem Destillationsapparat nach oben. Der Dampf kondensiert im Liebig-Kühler
und kann dann in einem Erlenmeyerkolben aufgefangen werden.
Beispiel:
Trennung einer Salzlösung.
b) Fraktionierte
Destillation
Mittels einer fraktionierten Destillation kann man mehrere ineinander
lösliche Flüssigkeiten trennen. Hierzu braucht man einen besonderen
Glasapparat, ein Destillationsgerät mit einer Vigreux-Kolonne.
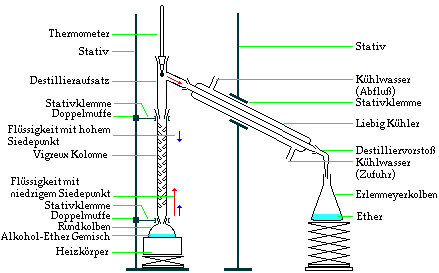
In einem ersten Schritt wird das Stoffgemenge langsam erhitzt. Die
Flüssigkeit mit der kleinsten Siedetemperatur steigt als Erste als Dampf in
dem Destillationsapparat nach oben. Die Vigreux-Kolonne erlaubt dabei ein
langsames aber stetes Ansteigen der Temperatur. Durch diese feinen
Temperaturunterschiede wird auch die Trennung von Flüssigkeiten mit relativ
kleinen Siedepunktunterschieden möglich. Der Dampf kondensiert im
Liebig-Kühler und kann dann in einem Erlenmeyerkolben aufgefangen werden.
Beispiel:
Trennung eines Alkohol-Ether-Gemenges.
9. Chromatografieren
Durch Chromatografie
kann man sehr komplizierte Gemische in ihre Bestandteile auftrennen.
Beispiel:
Auftrennung eines Farbstoffgemisches.
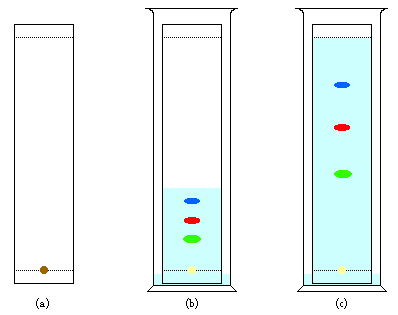
a. mit Hilfe eines
Kapillars bringt man eine
geringe Menge Gemisch auf Chromatografiepapier und lässt trocknen.
b. Dann gibt man das Chromatografiepapier in einen schließbaren
Glasbehälter, welcher ein Fließmittel (Gemisch von Lösungsmitteln) enthält.
Beim Aufsteigen des Fließmittels werden die verschiedenen Farbstoffe
unterschiedlich weit mitgerissen. Je weniger ein Stoff von dem
Chromatografiepapier zurückgehalten wird, je weiter wird er vom Fließmittel
mitgenommen.
c. Wenn das Fließmittel die obere Markierung erreicht hat, wird die
Chromatografie durch Herausnahme aus dem Glasbehälter und anschließendem
Trocknen beendet.
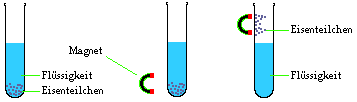
10. Trennung mittels eines Magneten
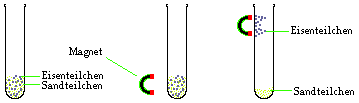
Eisen kann man mithilfe
eines Magneten von anderen Feststoffen oder Flüssigkeiten abtrennen.
Beispiel 1: Trennung von Eisenpulver und feinem Sand
Beispiel 2: Trennung von Eisenpulver und einer Flüssigkeit